
Bilastina vs Levocetirizina
La urticaria crónica constituye una patología cutánea frecuente, caracterizada por la aparición recurrente de habones pruriginosos que, en casos graves, pueden provocar una importante discapacidad (1). En numerosos casos la enfermedad puede catalogarse como idiopática (2), ya que la etiología permanece desconocida o infrecuentemente identificada (1, 3). La urticaria crónica (UC), en particular, presenta una prevalencia global de 0,5-1,0% en distintas poblaciones (3, 4). Se define por la presencia cotidiana, o casi diaria, de habones y prurito durante un mínimo de 6 semanas, pudiendo ocasionar grave deterioro funcional y afectar negativamente la calidad de vida (1, 5). De hecho, se ha sugerido que el impacto sintomático de la UIC en los pacientes podría asemejarse al observado en algunos ancianos con cardiopatía isquémica (6). Aunque se desconozcan los desencadenantes etiológicos en la UC, existen evidencias de que en el 30-50% de los casos subyace un mecanismo de autoinmunidad mediado por autoanticuerpos IgG.
La activación de los receptores de alta afinidad IgE en basófilos y mastocitos dérmicos puede conducir a la liberación de mediadores proinflamatorios como histamina, eicosanoides, citocinas y proteasas. Estas sustancias están implicadas en la patogénesis de la urticaria y el angioedema (1, 3).
"
Para comparar la eficacia y seguridad de bilastina vs levocetirizina se realiza un estudio en el que se reclutó a pacientes de entre 18 y 65 años con antecedentes documentados de urticaria crónica espontánea, sin factores inducibles conocidos o causas claras".
Dado que la histamina derivada de mastocitos dérmicos se asocia típicamente al desarrollo de prurito, edema y eritema, el tratamiento de primera línea para la urticaria crónica (UC) han sido tradicionalmente los antihistamínicos H1(7). Esta práctica ha sido recientemente respaldada y recomendada por un Consenso Internacional sobre el abordaje de la urticaria (8).
La bilastina es un novedoso antihistamínico H1 desarrollado para el tratamiento sintomático de la UC, rinitis alérgica estacional (RAE) y rinitis alérgica perenne (9). Estudios farmacológicos revelan que la bilastina posee una potente y selectiva actividad antagonista sobre receptores H1, con propiedades antihistamínicas y antialérgicas demostradas tanto in vitro como in vivo (10,11). Además, presenta un rápido inicio de acción y una prolongada duración del efecto (24 h) (12), con escaso metabolismo hepático (13) y eliminación principalmente fecal (9,14). Ensayos en voluntarios sanos (12,15–17) y en pacientes con rinitis alérgica (18,19) indican que la bilastina constituye una opción segura y altamente eficaz para el alivio sintomático de estas afecciones, a dosis terapéutica de 20 mg.

Bilastina vs Levocetirizina
Para comparar la eficacia y seguridad de bilastina vs levocetirizina se realiza un estudio en el que se reclutó a pacientes de entre 18 y 65 años con antecedentes documentados de urticaria crónica espontánea, sin factores inducibles conocidos o causas claras. Un Puntaje de Actividad de Urticaria ≥16 (esto es, urticaria moderada a severa) en la visita de aleatorización (día 0, visita 2) fue el criterio de elegibilidad adicional. Los criterios de exclusión fueron antecedentes de dermatosis incluyendo dermografismo, urticaria física, angioedema hereditario, alergia a alimentos o drogas, urticaria de contacto, enfermedades del colágeno vascular y dermatitis atópica, desórdenes autoinmunes sistémicos y enfermedad de Hodgkin.
También fueron excluidos pacientes que habían tomado corticoesteroides sistémicos o tópicos dentro de las 4 semanas previas, o cualquier antihistamínico oral dentro de las 72 horas previas a la visita de aleatorización, o que tuvieran cualquier causa conocida de urticaria como infecciones respiratorias/gastrointestinales o infestaciones parasitarias. Asimismo fueron excluidas mujeres embarazadas o lactando y pacientes con historia conocida de hipersensibilidad a antihistamínicos.
Fue un ensayo clínico aleatorizado (1:1), doble ciego, controlado con tratamiento activo, de grupos paralelos, en un centro de atención terciaria en el este de la India durante un período de 6 meses. El estudio fue aprobado por el Comité de Ética Institucional y realizado cumpliendo estrictamente con los principios éticos de la Declaración de Helsinki modificada de 1964 y las normas de Buenas Prácticas Clínicas de la Conferencia Internacional de Armonización (ICH).
Los pacientes fueron examinados para determinar su elegibilidad, el diagnóstico de UC y la gravedad de los síntomas el Día -7 (visita de detección, visita 1) y se les proporcionaron diarios para registrar su Puntuación de Actividad de Urticaria de 7 días (UA7) y regresar después de una semana.
Se utilizó una tabla de números aleatorios generada por ordenador para realizar una aleatorización simple con asignación 1:1 y dividir a los pacientes equitativamente en dos grupos. Los medicamentos del estudio fueron envueltos en blísteres idénticos de aluminio (para que los comprimidos no fueran identificables a la luz) y suministrados dentro de sobres opacos sellados con números de serie secuenciales (SNOSE) para lograr ocultamiento de la asignación y enmascaramiento de los pacientes. Sobres idénticos fueron codificados como “medicamento A” y “medicamento B” por el dispensador de medicamentos, manteniendo los códigos de forma segura solo para abrirse en caso de eventos adversos graves. Otro dermatólogo evaluó los parámetros del estudio, sentado en una sala separada y sin participar en la aleatorización o dispensación de medicamentos, haciendo el ensayo doble ciego.
La medida principal de efectividad fue la mejoría clínica y de síntomas, reflejada por los cambios en la Puntuación de Actividad de Urticaria, desde el inicio hasta el final del tratamiento, durante 42 días. Es un sistema sencillo y validado que se basa en evaluar una vez al día, durante 7 días, la intensidad del picor y el número de ronchas. Luego se suman las puntuaciones diarias (de 0 a 6) para obtener la puntuación semanal, que va de 0 (sin picazón ni ronchas) hasta 42 (síntomas máximos). Según esta puntuación la enfermedad se clasifica en: bien controlada (≤6), leve (7-15), moderada (16-27) o grave (28-42).
La seguridad de bilastina y el medicamento de comparación se evaluó en base a la aparición de eventos adversos durante el tratamiento, ya sea reportados espontáneamente por los pacientes o identificados por el dermatólogo en cada visita de seguimiento. Se realizaron exámenes bioquímicos de rutina y electrocardiogramas de 12 derivaciones el día 0 (basal) y el día 42 (visita final del tratamiento).
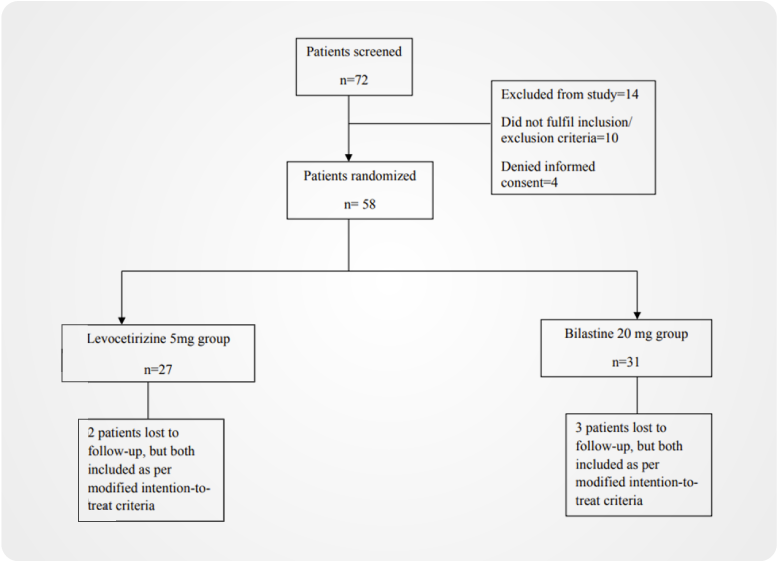
Inicialmente evaluamos a 72 pacientes, de los cuales 58 fueron aleatorizados en alguno de los dos grupos y sus datos analizados según el criterio modificado de intención de tratar (ITT), mientras que 53 (91,4%) completaron el estudio. Cinco pacientes del grupo de Levocetirizina (2) y del grupo de Bilastina (3) se perdieron durante el seguimiento. La Figura 1 muestra la disposición de los participantes del estudio.
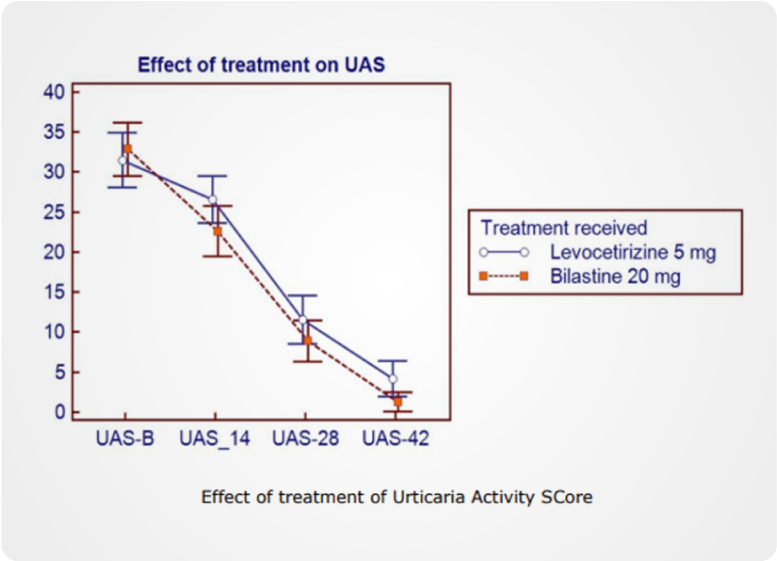
Efecto del tratamiento en la puntuación de actividad de urticaria a 7 días.
En los dos grupos, se redujo significativamente desde la primera semana de tratamiento en adelante, comparado con la puntuación inicial.
La bilastina 20mg disminuyó la urticaria en un promedio según la escala de puntuación de 32,9 al inicio a 1,3 al día 42 vs la levocetirizina 5mg la redujo de 31,5 a 4,1. Por lo tanto, la reducción de la medición de urticaria fue mayor con bilastina.
Al final del estudio, la reducción de la urticaria fue significativamente más baja en el grupo de bilastina que en el de levocetirizina (1,3 vs 4,1).
En el grupo de bilastina, 80,6% lograron controlar bien la urticaria al final, comparado con 51,9% en el grupo de levocetirizina con una diferencia de 28,7% a favor de bilastina. Esta diferencia fue estadísticamente significativa.
Referencias
- Kozel MMA, Sabroe RA. Chronic Urti- caria. Aetiology, management and current future treatment options. Drugs 2004;64:2515–2536.
- Kulthanan K, Jiamton S, Thumpimukva- tana N, Pinkaew S. Chronic idiopathic urti- caria: prevalence and clinical course. J Dermatol 2007;34:294–301.
- Greaves MW. Chronic idiopathic urticaria. Curr Opin Allergy Clin Immunol 2003;3:363– 368.
- Powell RJ, Du Toit GL, Siddique N, Leech SC, Dixon TA, Clark AT et al. BSACI guidelines for the management of chronic urticaria and angio-oedema. Clin Exp Allergy 2007;37:631–650.
- Zuberbier T, Bindslev-Jensen C, Canonica W, Grattan CEH, Greaves MW, Henz BM et al. EAACI/GA LEN/EDF guideline: def-2inition, classification and diagnosis of urti- caria. Allergy 2006;61:316–320.
- O’Donnell BF, Lawlor F, Simpson J, Mor- gan M, Greaves MW. The impact of chronic urticaria on the quality of life. Br J Derma- tol 1997;136:197–201.
- Monroe E. Review of H antihistamines in1the treatment of chronic idiopathic urticaria. Cutis 2005;76:119–126.
- Zuberbier T, Bindslev-Jensen C, Canonica W, Grattan CEH, Greaves MW, Henz BM et al. EAACI/GA2LEN/EDF guideline: management of urticaria. Allergy 2006;61:321–331.
- Faes Farma SA. Bilastine (F-96221-BMI): a novel antihistamine compound for the treat- ment of allergic rhinitis and chronic idio-Drugpathicurticaria.InvestigationalBrochure (Version 9 July 2008). Data on file;http://www.faes.es (last accessed August2009)
- Corco´ stegui R, Labeaga L, Innera´ rity A, Berisa A, Orjales A. Preclinical pharmacol- ogy of bilastine, a new selective histamine H1 receptor antagonist: receptor selectivity and in vitro antihistaminic activity. Drugs R D 2005;6:371–384.
- Corco´ stegui R, Labeaga L, Innera´ rity A, Berisa A, Orjales A. In vivo pharmacologi- cal characterisation of bilastine, a potent and selective histamine H1 receptor antago- nist. Drugs R D 2006;7:219–231.
- Sologuren A, Valiente R, Crean C, McLav- erty A. Relationship of dose to inhibition of wheal and flare for 5 doses of bilastine and 10 mg cetirizine. J Clin Pharmacol 2007; 47: 1198 (abstract 69).
- Lucero ML, Orjales A, Morag N. In vitro hepatic metabolism of [14 C] bilastine. Drug Metabol Rev 2007; 39 (Suppl. 1): 114 (abstract 160).
- Mumford R, Allan A, Hoey R, Patterson A, Orjales A, Lucero ML et al. The disposition, metabolism and elimination in rats of bilas- tine, a potent selective H1 receptor antago- nist. Drug Metabol Rev 2007; 39 (Suppl. 1): 200–201 (abstract 282).
- Crean C, Roupe K, Sologuren A, Valiente R. The pharmacokinetics of bilastine after single and 14 days once daily administration. Basic Clin Pharmacol Toxicol 2007;101(Sup- pl. 1): 148.
- Garcıa-Gea C, Martı´ nez-Colomer J, Antoni- joan RM, Valiente R, Barbanoj MJ. Com- parison of peripheral and central effects of single and repeated oral dose administra- tions of bilastine, a new H1 antihistamine: a dose-range study in healthy volunteers with hydroxyzine and placebo as control treat- ments. J Clin Psychopharmacol 2008;28:675– 685.
- Sologuren A, Valiente R, Allison M, Tyl B. Lack of significant effect of bilastine on ven- tricular repolarization. A thorough QT/QTc study. Allergy 2008;63(Suppl. 88):85.
- Ivan P, Dimitrov V, Gorine NM et al. Com- parison of the efficacy and safety of bilastine 20mg versus desloratadine 5mg in seasonal allergic rhinitis patients. Allergy 2009;64:158–165.
- Kuna P, Bachert C, Nowacki Z, van Cau- wenberge P, Agache I, Fouquert L et al. The Bilastine International Working Group. Efficacy and safety of bilastine 20 mg com- pared with cetirizine 10 mg and placebo for the symptomatic treatment of seasonal aller- gic rhinitis: a randomized, double-blind, par- allel-group study. Clin Exp Allergy 2009;39:1338–1347.





















